Para que os projetos de engenharia metabólica sejam bem sucedidos, os cientistas precisam alterar diversas características nos organismos hospedeiros. Inserir os genes da via metabólica de interesse, remover genes que causam efeitos indesejados ou que acarretam no desvio da via, incluir genes de resistência às condições de cultivo (como o baixo pH do meio, por exemplo), são algumas opções de manipulação genética que podemos realizar.
De certa forma, encarar um projeto desses é como encarar a montagem de um brinquedo de LEGO. Temos várias peças (ou partes genéticas), onde cada uma tem uma função diferente, e elas precisam ser devidamente encaixadas para que o brinquedo seja montado de forma correta, ou seja, para que o sistema funcione da maneira que deveria.
Se você quiser saber mais sobre a engenharia metabólica e outras etapas da execução de um projeto nessa área, leia os demais textos da nossa Série Especial sobre Engenharia Metabólica!
Para começar a montar o nosso brinquedo de LEGO, devemos primeiramente organizar as peças em categorias, separando cada uma delas de acordo com sua função. Num projeto de engenharia metabólica, quem surge para fazer essa categorização e nos ajudar a organizar nossas “peças de LEGO” (melhor dizendo, partes genéticas, ou building blocks em inglês) é a Biologia Sintética. O papel da área é caracterizar a maior quantidade possível dessas partes, para que possamos ter algo como se fosse um “catálogo de partes genéticas”. Assim, a construção do nosso “LEGO genético” fica cada vez mais fácil e mais intuitiva.
Conhecendo alguns tipos de partes genéticas
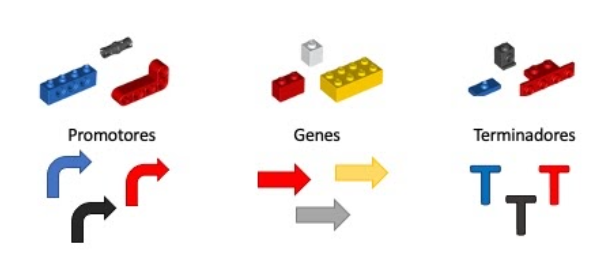
As partes genéticas a que nos referimos são as partes necessárias para que nosso sistema de expressão funcione. Algumas dessas partes são:
(1) Nossos genes de interesse: sequências de DNA que vão ser traduzidas em proteínas e enzimas para que a nossa via metabólica funcione como desejamos. Serão escolhidos cuidadosamente depois de ponderar tudo que aprendemos na série sobre Engenharia Metabólica.
(2) Promotores: sequências de DNA que controlam a expressão dos genes. Diferentes promotores podem modular não somente quando e se o nosso gene de interesse vai ser expresso, mas também qual será a intensidade da expressão. Podemos construir nosso sistema de expressão com um promotor forte, resultando em uma alta expressão, ou um promotor fraco, resultando em uma baixa expressão do gene de interesse. A segunda opção é mais relevante quando o produto resultante da expressão é tóxico para a célula, por exemplo, ou ainda para evitar o burden metabólico (como abordado neste outro texto da série). Além disso, outra maneira de controlar a expressão dos genes é utilizando promotores induzíveis. Estes são promotores que precisam de moléculas ou sinais específicos para serem ativados, e estes ativadores podem ser adicionados ao meio de cultivo conforme necessário.
(3) Terminadores, sequências que determinam o fim da transcrição daquele gene. As sequências de terminação de transcrição são importantes para garantir o isolamento de cada parte do sistema, evitando assim interações regulatórias indesejadas.
Quanto mais promotores, genes e terminadores nós testarmos, maior vai ser nosso “catálogo de partes”. Assim, podemos montar diversos brinquedos de LEGO diferentes, até que um deles se comporte da forma que queremos.
Algumas outras partes genéticas também são necessárias para montar nosso sistema. Um exemplo são os genes de seleção, que podem ser genes de resistência à antibióticos ou genes que fazem o organismo consumir fontes de nutrientes que normalmente não são capazes. Esses genes de seleção também precisam de seu próprio promotor e terminador. Outros exemplos são o sítio de múltipla clonagem (MCS, do inglês Multiple Cloning Site), origens de replicação e transferência, e sequências de homologia. Se estiver muito curioso, este artigo aqui conta um pouco mais sobre essas outras partes. Vamos explicar mais sobre elas no próximo texto da série sobre Engenharia Metabólica, onde vamos também aprender como inserir essas partes nas células hospedeiras por meio de diferentes técnicas.
E como unimos essas partes para montar nosso LEGO?
Diferentemente das peças de LEGO, as partes genéticas que aprendemos acima não podem simplesmente serem encaixadas umas nas outras. Para unirmos essas partes e construirmos um sistema de expressão, contamos com uma metodologia chamada de clonagem de DNA. A clonagem vem sendo utilizada desde os anos 70, e consiste justamente em unir partes genéticas em vetores plasmidiais para se tornarem sistema de expressão de genes. Diversos métodos de clonagem vêm sendo desenvolvidos desde então, como ligação por enzimas de restrição, recombinação, Golden Gate Cloning, Gibson Assembly, entre outros. Cada um desses métodos possui suas próprias vantagens e desvantagens.
Figura 3. Para unir as peças de LEGO, precisamos de um método de clonagem de DNA. Os métodos de clonagem unem as partes genéticas e formam o plasmídeo recombinante. Imagem adaptada de Khan Academy: Clonagem de DNA.
Pronto! Agora já sabemos quais são as principais partes genéticas que precisamos para começar a montar o LEGO genético e também como fazemos para unir as peças. Com o LEGO montado, agora é hora de escolher o organismo de interesse e começar a manipulação genética dele. Com esses sistemas genéticos, podemos deletar genes, alterar vias metabólicas inteiras, acrescentar novas características, novas resistências, dentre outras possibilidades. A imaginação é o limite! Fiquem ligados aqui no Profissão Biotec para não perder as dicas de como escolher o organismo e de como inserir o LEGO montado na forma de plasmídeo ou por inserção genômica no DNA do hospedeiro.


Cite este artigo:
NORA, Luísa Czamanski;SILVA-ROCHA, Rafael. Ferramentas genéticas usadas para engenheirar microrganismos: partes genéticas. Revista Blog do profissão Biotec, v7, 2021.
Referências:
NORA, Luísa Czamanski; WESTMANN, Cauã Antunes; MARTINS-SANTANA, Leonardo; ALVES, Luana de Fátima; MONTEIRO, Lummy Maria Oliveira; GUAZZARONI, María-Eugenia; SILVA-ROCHA, Rafael. The art of vector engineering: towards the construction of next-generation genetic tools. Microbial Biotechnology, v. 12, n. 1, p. 125-147. 2018. Wiley. http://dx.doi.org/10.1111/1751-7915.13318.
Xiangyang Liu, Sanjan T P Gupta, Devesh Bhimsaria, Jennifer L Reed, José A Rodríguez-Martínez, Aseem Z Ansari, Srivatsan Raman, De novo design of programmable inducible promoters, Nucleic Acids Research, Volume 47, Issue 19, 04 November 2019, Pages 10452–10463, https://doi.org/10.1093/nar/gkz772




